|

 |
|  | |||||||||||||||||||||||||||||||||||||||||
Noticias | Médicas | PatologíaLa ciencia avanza en el estudio de anticuerpos relacionados con la «enfermedad de las vacas locas»Las enfermedades priónicas son enfermedades neurodegenerativas que afectan tanto a animales como a humanos. Se desarrollan cuando una proteína natural del cerebro denominada PrP entra en contacto con los priones infecciosos. Publicado: Martes, 10/3/2009 - 20:7 | 2722 visitas.
Investigadores de la Universidad de Liverpool (Reino Unido) han desentrañado la estructura atómica del punto de unión entre una proteína del cerebro y un anticuerpo que podría ser vital para encontrar una cura para enfermedades neurodegenerativas como la variante de la enfermedad de Creutzfeldt-Jakob (ECJ). Sus descubrimientos se han publicado en la revista Proceedings of the National Academy of Sciences (PNAS). La variante de la ECJ ha recibido la atención de los medios de comunicación durante las dos últimas décadas debido a su capacidad para transmitirse a los humanos desde el ganado bovino, en el que causa la enfermedad neurodegenerativa de la Encefalopatía Espongiforme Bovina (EEB). La ECJ es una enfermedad neurodegenerativa rara que puede desarrollarse en humanos tras consumir productos cárnicos vacunos infectados con la EEB. La responsable del desarrollo de la variante de la ECJ es un tipo de proteína poco habitual denominada prión. Los priones pueden provocar una serie de enfermedades conocidas como encefalopatías espongiformes transmisibles (EET), entre ellas la enfermedad de las vacas locas en el ganado vacuno y la tembladera en las ovejas. Las enfermedades priónicas son enfermedades neurodegenerativas que afectan tanto a animales como a humanos. Se desarrollan cuando una proteína natural del cerebro denominada PrP entra en contacto con los priones infecciosos. Los priones transforman las proteínas PrP de tal modo que se acaban por acumular en el cerebro y provocan la muerte de las neuronas. Los científicos de Liverpool investigan si la inmunización con ciertos anticuerpos que puedan adherirse a las PrP podría servir para tratar la enfermedad e incluso prevenir su desarrollo. Para adquirir una visión más clara de la relación entre los anticuerpos y las PrP, los científicos emplearon cristalografía por rayos X. Construyeron una imagen tridimensional de la manera en la que un anticuerpo llamado ICSM18 se adheriría a las proteínas priónicas y a las células PrP. Samar Hasnain, profesor de biofísica molecular de la Universidad de Liverpool, informó que «para establecer dónde se adhiere el anticuerpo a la proteína utilizamos cristalografía por rayos X, que fue desarrollada por el premio Nobel Max Perutz. Curiosamente, hemos descubierto que el punto en el que la proteína y el anticuerpo se unen es el mismo donde científicos de la Unidad Priónica del Consejo de Investigación Médica (MRC) habían identificado un aminoácido único, el cual ahora sabemos que influye considerablemente en la susceptibilidad del paciente a sufrir una enfermedad priónica.» Científicos de la Unidad Priónica del MRC del University College de Londres (Reino Unido) colaboraron con los investigadores de la Universidad de Liverpool. Descubrieron que el anticuerpo ICSM18 no sólo ayuda a impedir que las neuronas se infecten con priones, sino que también podría curar los daños causados por la enfermedad en sus fases iniciales. El profesor John Collinge, director de la Unidad Priónica del MRC, afirmó que «hemos demostrado que el ICSM18 posee el mayor potencial terapéutico en estudios animales y celulares, pero todavía hemos de averiguar el efecto que tiene en personas que sufren la variante de la ECJ u otras enfermedades priónicas. Ya estamos preparando versiones humanas de los anticuerpos para probarlos en personas.»
| NoticiasImágenes
Videos
Artículos
EntradasLibros
| ||||||||||||||||||||||||||||||||||||||||||



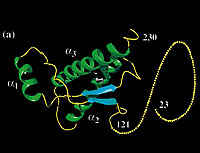
 Imagen: Agencias / Internet
Imagen: Agencias / Internet